Na pierwszym wykazie innowacyjnych technologii lekowych, którą AOTMiT ma opublikować na potrzeby Funduszu Medycznego, mogą się znaleźć nawet 42 cząsteczki. Do 20 leków, traktowanych jako pojedyncza technologia lekowa (lek+wskazanie), zarejestrowanych po 1 stycznia 2020 r., przy odpowiedniej interpretacji ustawy refundacyjnej można dodać także 22 kolejne technologie których wskazania zostały ostatnio poszerzone lub rozszerzono docelową populację (np. o dzieci) – wskazują analizy ekspertów HTA Consulting.

Robert Plisko, prezes HTA Consulting – Od wielu lat w Polsce prowadzona jest dyskusja nad zwiększeniem dostępności do nowych technologii lekowych, szczególnie w leczeniu chorób rzadkich oraz onkologicznych. 26 listopada 2020 r. weszła ustawa o Funduszu Medycznym, z inicjatywy Prezydenta PR , która znowelizowała zapisy ustawy refundacyjnej. Wprowadziła ona nowe ścieżki refundacyjne dla technologii lekowych o wysokim poziomie innowacyjności oraz wysokiej wartości klinicznej.
Zgodnie z zapisami ustawy o Funduszu Medycznym pierwszy wykaz leków po ocenie AOTMiT o wysokim poziomie innowacyjności dla terapii w onkologii i chorobach rzadkich ma zostać opublikowany w dniu 26 lutego 2021. Ma być on podstawą stworzenia listy MZ po konsultacjach, wymaganych zgodnie z ustawą. Na pierwszym wykazie mogą zostać umieszczone technologie lekowe dopuszczone do obrotu w procedurze centralnej w Unii Europejskiej od 1 stycznia 2020 r. i których producenci nie złożyli wniosków refundacyjnych. Do zadań AOTMiT należy ustalenie wykazu z technologiami lekowymi wraz z określeniem poziomu ich innowacyjności. Dodatkowo w ramach wykazu mają być przedstawione szczegóły populacji docelowych oraz zakres danych gromadzonych w rejestrze medycznym, w tym między przede wszystkim wskaźniki oceny efektywności terapii i oczekiwane wyniki terapii.
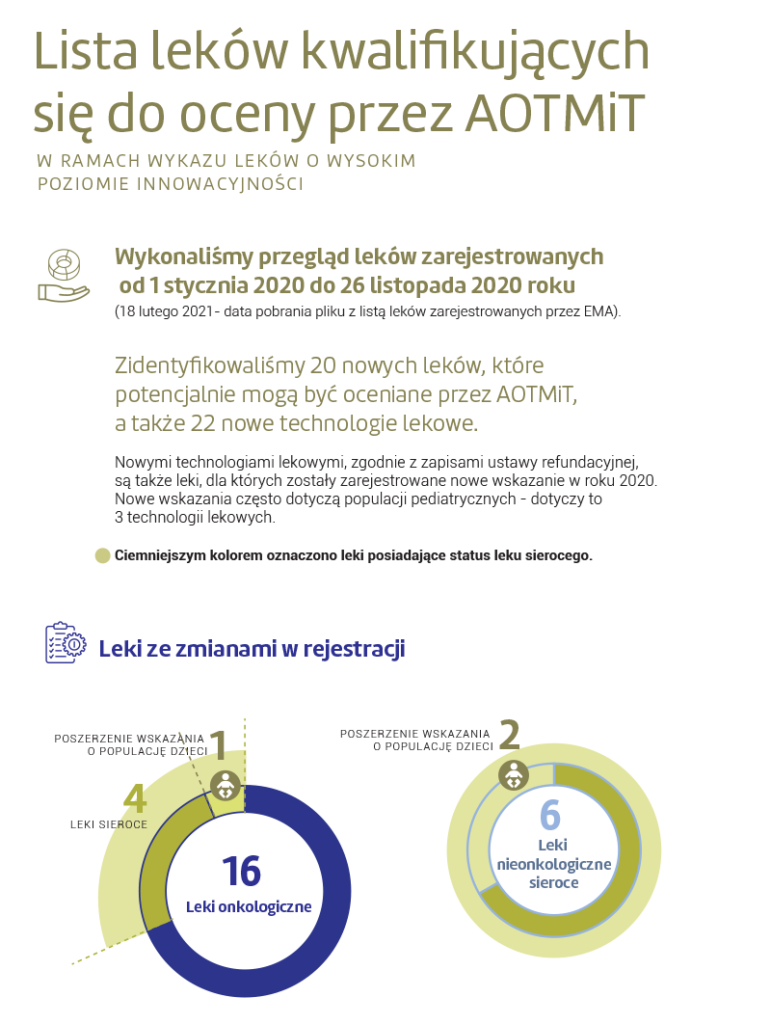
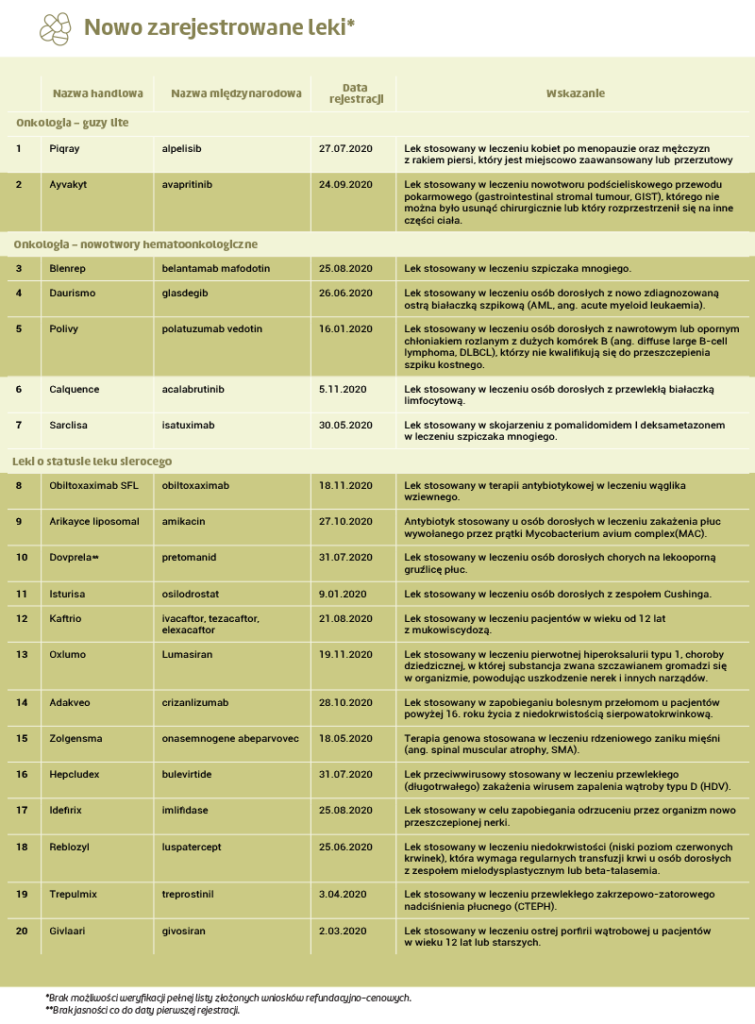
Zidentyfikowaliśmy 20 nowych leków, które potencjalnie mogą być oceniane przez AOTMiT oraz 22 nowe wskazania dla wcześniej zarejestrowanych technologii lekowych. Nowymi technologiami lekowymi, zgodnie z zapisami ustawy refundacyjnej, są bowiem także leki, dla których zostały zarejestrowane nowe wskazania w roku 2020. Nowe wskazania często dotyczą populacji pediatrycznych – dotyczy to 3 technologii lekowych. Nasze zestawienie obejmuje okres od 1 stycznia 2020 do 26 listopada 2020, ponieważ według informacji z AOTMiT będzie ona rozpatrywać rejestracje sprzed tej daty; 18 lutego pobraliśmy plik z listą leków zarejestrowanych na stronie EMA.
Opisane w ustawie o Funduszu Medycznym kryteria przygotowywania przez AOTMiT wykazu technologii lekowych o wysokim stopniu innowacyjności wskazują, że mają to być leki stosowane w leczeniu chorób nowotworowych lub rzadkich. Mają także dotyczyć niezaspokojonych potrzeb medycznych. Na liście nie mogą być umieszczone leki, których dotyczą złożone już wnioski o refundację. Wykaz technologii lekowych o wysokim stopniu innowacyjności, finansowanych w ramach Funduszu Medycznego, przygotowany przez AOTMiT będzie jeszcze konsultowany przez Ministerstwo Zdrowia – z Radą Przejrzystości, Rzecznikiem Praw Pacjenta oraz konsultantami krajowymi z odpowiednich dziedzin medycyny.
© mZdrowie.pl








































































